MiR-204-3p hamował proliferację komórek raka pęcherza moczowego poprzez modulowanie glikolizy za pośrednictwem dehydrogenazy mleczanowej
- 1 Zakład Urologii, Centrum Urologii Shenzhen w minimalnym stopniu inwazyjne, Drugie kliniczne medyczne kolegium uniwersytetu Jinan, Shenzhen People's Hospital, Pierwszy afiliowany szpital South University of Science and Technology of China, Shenzhen, Chiny
- 2 Platforma usług publicznych w Shenzhen w zakresie precyzyjnej medycyny nowotworowej i diagnostyki molekularnej, centrum urologii Shenzhen o minimalnej inwazyjności, drugie kliniczne medyczne kolegium Uniwersytetu Jinan, Shenzhen People's Hospital, pierwszy szpital stowarzyszony z południowym uniwersytetem nauki i technologii w Chinach, Shenzhen, Chiny
- 3 Centrum badań medycznych klinicznych, Centrum urologii w Shenzhen, minimalnie inwazyjne centrum inżynieryjne, Druga kliniczna szkoła medyczna Uniwersytetu Jinan, Szpital Ludowy w Shenzhen, Pierwszy Szpital Stowarzyszony Południowego Uniwersytetu Nauki i Technologii w Chinach, Shenzhen, Chiny
MikroRNA (miRNA) to endogenne niekodujące RNA, które negatywnie regulują ekspresję docelowych mRNA. Coraz więcej dowodów sugeruje, że miRNA działają jako supresory nowotworów lub onkogeny, zakłócając postęp nowotworów. Tutaj pokazaliśmy, że miR-204-3p był zmniejszony w tkankach raka pęcherza i liniach komórkowych. Regulacja w dół miR-204-3p była istotnie związana ze złym rokowaniem u pacjentów z rakiem pęcherza. Nadekspresja miR-204-3p hamowała proliferację i indukowała apoptozę w komórkach raka pęcherza moczowego. Ponadto stwierdzono, że miR-204-3p wiąże się z regionem nieulegającym translacji 3'-U (UTR) dehydrogenazy mleczanowej (LDHA), co w konsekwencji zmniejsza ekspresję zarówno mRNA, jak i białka LDHA. Co ciekawe, nadekspresja miR-204-3p zmniejszała zużycie glukozy i produkcję mleczanu komórek raka pęcherza moczowego. Nadekspresja LDHA złagodziła zahamowanie wzrostu i zwiększenie apoptozy komórek przez miR-204-3p w komórkach raka pęcherza moczowego. Wyniki te wykazały, że miR-204-3p negatywnie moduluje proliferację komórek raka pęcherza moczowego poprzez celowanie w glikolizę za pośrednictwem LDHA. MiR-204-3p może być obiecującym kandydatem do projektowania leków przeciwnowotworowych.
Wprowadzenie
Rak pęcherza moczowego (BC) jest jednym z najczęstszych nowotworów w układzie urologicznym ( 1 ). Istnieje około 356.000 nowych zachorowań i zgonów rocznie 145,000 całego świata ( 1 - 3 ). Wysokie występowanie i śmiertelność BC sprawiają, że jest to duże zagrożenie dla zdrowia pacjentów. Mimo znacznego postępu w leczeniu BC, w tym chirurgicznej resekcji i chemioterapii, 5-letnie całkowite przeżycie BC pozostaje słabe ( 4 , 5 ). Dlatego pilnie należy zidentyfikować nowe biomarkery i cele BC.
MikroRNA (miRNA) to klasa jednoniciowych niekodujących RNA o długości 22–24 nukleotydów ( 6 , 7 ). MiRNA negatywnie regulują ekspresję genu poprzez wiązanie z regionem nieulegającym translacji 3 '(UTR) celów, co prowadzi do degradacji lub hamowania translacji mRNA ( 8 ). Donosi się, że MiRNA są zaangażowane zarówno w stanach fizjologicznych, jak i patologicznych, w tym w proliferację komórek, różnicowanie i apoptozę ( 9 , 10 ). Najnowsze badania wykazały, że nieprawidłowa ekspresja miRNA wiązało się z powstawaniem nowotworu BCS ( 9 - 12). Dlatego wykrycie obfitości miRNA może dostarczyć nowych dowodów na diagnozę BC i przynieść korzyści wynikom u pacjentów z rakiem. Aby uzyskać pełny obraz na temat ekspresji miRNA w BC, przejrzeliśmy poprzednie publikacje dotyczące zmienionych miRNA w BC i przeprowadziliśmy metaanalizę. Dane wykazały, że miR-204-3p był znacznie obniżony w supernatancie moczu u pacjentów z BC ( 13 ). Co ciekawe, często stwierdzono, że miR-204-3p ma obniżoną regulację w nowotworach, które działały jako supresor guza w nowotworze ( 14 ). Nieprawidłową ekspresję miR-204-3p zaobserwowano w guzach zrębowych przewodu pokarmowego, raku piersi i raku wątrobowokomórkowym ( 15 , 16)). Jednak ekspresja i funkcja miR-204-3p w BC pozostają w dużej mierze nieznane.
Tlenowych glikolizy uznano za wyraźną cechę charakterystyczną komórek nowotworowych, co oznacza, że komórki rakowe addictively zależą glikolizy w metabolizmie glukozy, nawet w warunkach bogatych w tlen ( 17 - 19 ). Dlatego zrozumienie mechanizmów, które przyczyniają się do procesu glikolizy, dostarczy nowych wskazówek dotyczących strategii terapeutycznych w leczeniu raka. Dehydrogenaza mleczanowa (LDHA) jest kluczowym enzymem glikolizy, który katalizuje produkcję mleczanu ( 20 ). Regulacja w górę LDHA stwierdzono w wielu rakach ludzkich, co jest związane ze wzrostem komórek, przerzutów i złym rokowaniem u pacjentów z rakiem ( 21 - 24). W szczególności, doniesiono, że miRNA celują w LDHA i negatywnie regulują ekspresję LDHA. Na przykład represja LDHA przez miR-34a hamowała glikolizę i hamowała wzrost komórek raka piersi ( 20 ). Ostatnie badania wykazały, że miR-142-3p celował w LDHA, co zmniejszało glikolizę i wzrost komórek HCC ( 25 ). Raporty te sugerują, że ujemna modulacja LDHA przez miRNA jest ważną strategią regulującą postęp nowotworów.
W tym badaniu zbadaliśmy funkcję miR-204-3p w BC. Dane wykazały, że miR-204-3p był obniżony w tkankach i liniach komórkowych BC. Nadekspresja miR-204-3p zmniejszała proliferację komórek BC poprzez modulowanie glikolizy za pośrednictwem LDHA.
Materiały i metody
Metaanaliza
Badania, które zgłosiły przemianę miRNA w BC, zostały przeszukane za pomocą baz danych Omnibus Gene Expression Omnibus (GBI) i EBI ArrayExpress w Narodowym Centrum Informacji Biotechnologicznej (NCBI) ze słowami kluczowymi „człowiek” i „pęcherz” i „miRNA”. W metaanalizie priorytetem były recenzowane publikacje, które badały ekspresję miRNA zarówno w BC, jak i w odpowiednich normalnych kontrolach. W badaniach bez danych grupy kontrolnej wykluczono tylko wyniki oparte na hodowli komórkowej. Ekstrakcja danych z wybranych publikacji zawierała imię i nazwisko pierwszego autora, czas publikacji, wielkość próby, wiek pacjenta, rodzaj przypadku, pochodzenie badanej populacji, stadium guza, metodę wykrywania oraz wartości odcięcia dla regulacji w dół lub w górę. Jakość publikacji została oceniona w skali Newcastle-Ottawa, który był ogólnie stosowany do oceny jakości badań nierandomizowanych w metaanalizach. Każdy artykuł został poddany ocenie za pomocą ośmiu metodologii z wynikiem w zakresie od 0 do 9. Wyższy wynik wskazywał na lepszą jakość publikacji. Artykuły z wynikiem 7 lub więcej zostały zrekrutowane do metaanalizy.
Próbki kliniczne i linie komórkowe
Łącznie 60 sparowanych BC i sąsiadujących z nimi normalnych tkanek uzyskano od pacjentów z BC, którzy przeszli operację w Szpitalu Ludowym w Shenzhen. Tkanki zostały niezależnie potwierdzone przez trzech patologów. Żaden z pacjentów nie otrzymał radioterapii ani chemioterapii przed resekcją chirurgiczną. Wszystkie tkanki utrzymywano w ciekłym azocie do momentu użycia. Wszystkie procedury eksperymentalne zostały zatwierdzone przez Komitet Etyki Badań Szpitala Ludowego w Shenzhen, a każdy pacjent podpisał świadomą pisemną zgodę.
Normalne ludzkie komórki urotelialne SV-HUC-1 zakupiono w Instytucie Badań Komórkowych Chińskiej Akademii Nauk (Szanghaj, Chiny). Linie komórkowe BC, w tym SW780, J82, UMUC3, 5637 i T24, zakupiono z American Type Culture Collection (ATCC, Rockville, MD, USA). Komórki hodowano w pożywce Roswell Park Memorial Institute (RPMI) -1640 (Gibco, Thermo Fisher Scientific, Carlsbad, Kalifornia, USA) uzupełnionej 10% płodową surowicą bydlęcą (FBS; Sigma-Aldrich, St. Louis, MO, USA), 100 jednostek / ml penicyliny i 100 mg / ml streptomycyny (lnvitrogen, Carlsbad, CA, USA) w 37 ° C z 5% cO 2 .
Ilościowa analiza PCR odwrotnej transkryptazy
MiRNA ekstrahowano z linii komórkowych lub tkanek pęcherza moczowego przy użyciu zestawu miRNeasy Mini Kit (QIAGEN, Hilden, Niemcy) zgodnie z instrukcją producenta; 0,5 μg RNA poddano odwrotnej transkrypcji do cDNA za pomocą Master Mix RT PrimeScript (Takara, Dalian, Chiny). Analizę PCR w czasie rzeczywistym przeprowadzono za pomocą SYBR Select Master Mix (Takara, Dalian, Chiny) na platformie ABI7500 (Applied Biosystems, Foster City, Kalifornia, USA). Ekspresję RNA U6 i GAPDH wykryto jako odpowiednią kontrolę endogenną. Poziom ekspresji miR-204-3p i LDHA został znormalizowany do U6 i GAPDH i obliczony przy użyciu 2 ΔΔCTmetoda. Startery były następujące: miR-204-3p, F, 5'-ACACTCCAGCTGGGGCTGGGAAGGCAAAGGG-3 'i R, 5'-CTCAACTGGTGTCGTGGA-3'; LDHA, F, 5′-AGCCCGATTCCGTTACCT-3 ′ i R, 5′-CACCAGCAACATTCATTCCA-3 ′; U6, F, 5′-CTCGCTTCGGCAGCACA-3 'i R, 5′-AACGCTTCACGAATTTGCGT-3'; i GAPDH, F, 5'-TGACGCTGGGGCTGGCATTG-3 'i R, 5'-GCTCTTGCTGGGGCTGGTGG-3'.
Żywotność komórek
Proliferację komórek BC z transfekcją kontrolnego miRNA lub miR-204-3p oceniano w teście Cell Counting Kit-8 (CCK-8, Beyotime, Szanghaj, Chiny). W skrócie, 10 μl odczynnika CCK-8 dodano do pożywki we wskazanych punktach czasowych 1, 2, 3, 4 i 5 dni i inkubowano przez 4 godziny w 37 ° C. Wartość absorbancji (gęstość optyczna [OD]) każdej studzienki przy 450 nm wykrywano za pomocą czytnika mikropłytek (Bio-Rad, CA, USA). Wyniki uzyskano z trzech niezależnych eksperymentów.
Tworzenie kolonii komórkowej
Komórki BC wyrażające wskazany miRNA zostały zaszczepione w 6-studzienkowej płytce o gęstości 1000 komórek na studzienkę. Komórki hodowano w pożywce RPMI-1640 przez 2 tygodnie. Następnie pożywkę odrzucono, a komórki przemyto dwukrotnie solą fizjologiczną buforowaną fosforanem (PBS). Komórki utrwalono metanolem przez 15 minut w temperaturze pokojowej (RT). Po przemyciu PBS kolonie zabarwiono 1% fioletem krystalicznym, a liczbę kolonii zliczono za pomocą mikroskopii świetlnej.
Western Blot
Białko ekstrahowano z komórek BC buforem do lizy NP-40 (150 mM NaCl, 1% NP-40, 50 mM Tris – HCl (pH 8,0) i 1 mM EDTA) w obecności inhibitora proteinazy ( Millipore, Braunschweig, Niemcy). Stężenie białka oceniono za pomocą zestawu do oznaczania kwasu bicynchoninowego (BCA) (Beyotime, Szanghaj, Chiny); 15 μg białek załadowano i rozdzielono za pomocą 15% elektroforezy w żelu poliakryloamidowym z dodecylosiarczanem sodu (SDS-PAGE), a następnie przeniesiono na membranę z difluorku poliwinylidenu (PVDF) (Millipore, Brunszwik, Niemcy). Membranę najpierw zablokowano 5% beztłuszczowym mlekiem w RT przez 1 godzinę, następnie inkubowano z pierwszorzędowymi przeciwciałami w RT przez 2 godziny i inkubowano membranę z kozim anty-mysim drugorzędowym przeciwciałem IgG (1: 3000, Bio- Rad, CA, USA), a następnie analizowane przy użyciu chemiluminescencyjnego substratu sprzężonego z peroksydazą chrzanową (HRP) (Millipore, Braunschweig, Niemcy). GAPDH zastosowano jako kontrolę ładowania. Przeciwciała, w tym anty-LDHA (# 2012, 1: 3,000, Cell Signaling Technology, Inc., Danvers, MA, USA) i anty-GAPDH (# 5174, 1: 3,000, Cell Signaling Technology, Inc., Danvers, MA, USA ) zostały uzyskane w celach handlowych.
Test reportera Lucyferazy
Dziki typ (WT) lub mutant (MUT) 3'-UTR LDHA zawierający domniemane miejsca wiązania miR-204-3p wstawiono do wektora pmiR-GLO. Komórki BC transfekowano kontrolnym naśladującym miRNA lub miR-204-3p w obecności wektora reporterowego lucyferazy. Po transfekcji przez 48 godzin komórki zebrano i aktywność lucyferazy określono za pomocą systemu reporterowego z podwójną lucyferazą (Promega, Madison, WI, USA). Eksperyment przeprowadzono w trzech egzemplarzach.
Pomiar zużycia glukozy i produkcji mleczanu
Komórki BC transfekowane odpowiednimi miRNA hodowano w pożywce RPMI-1640 bez czerwieni fenolowej (Gibco, Nowy Jork, Nowy Jork, USA) przez 24 godziny, a następnie pożywkę zebrano. Zużycie glukozy i wytwarzanie mleczanu określono przy użyciu zestawu do oznaczania glukozy (GAHK20-1KT; Sigma-Aldrich, USA) i zestawu do oznaczania mleczanu (BioVision, CA, USA), odpowiednio, zgodnie z instrukcjami producenta. Poziom białka w każdej grupie mierzono za pomocą zestawu testowego BCA (Beyotime, Szanghaj, Chiny) w celu normalizacji.
Analiza statystyczna
Wyniki przedstawiono jako średnią ± odchylenie standardowe z trzech niezależnych eksperymentów. Dane analizowano za pomocą oprogramowania SPSS 19.0 (SPSS Inc., Chicago, IL, USA). Istotne różnice między / między grupami leczenia analizowano przy użyciu niesparowanego testu t- Studenta lub jednokierunkowej ANOVA, a następnie testu post hoc Dunnetta . P <0,05 uznano za statystycznie znaczący.
Wyniki
MiR-204-3p był regulowany w dół w tkankach raka pęcherza i liniach komórkowych
Aby uzyskać pełny obraz ekspresji miRNA w BC, przeprowadzono metaanalizę miRNA przy użyciu poprzednich publikacji. Dane wykazały, że miR-204-3p był znacząco nieprawidłowo wyrażany w supernatancie moczu pacjentów z BC ( ryc. 1A ). Aby potwierdzić ten wynik, ekspresję miR-204-3p wykryto metodą ilościowej PCR z odwrotną transkryptazą (RT-qPCR) z parami tkanek BC i odpowiadającymi im normalnymi tkankami. Wynik pokazał, że poziom miR-204-3p był znacznie zmniejszony w tkankach BC w porównaniu z poziomem normalnych odpowiedników ( ryc. 1B ). Aby dodatkowo potwierdzić nieprawidłową ekspresję miR-204-3p w BC, zbadano obfitość miR-204-3p w kilku liniach komórkowych BC. Jak wskazano na rycinie 1CmiR-204-3p był znacznie zmniejszony w komórkach BC, w porównaniu z normalnymi komórkami, w tym SW780, J82, UMUC3, 5637 i T24. Wyniki te sugerują obniżenie regulacji miR-204-3p w BC. Aby dodatkowo scharakteryzować związek między ekspresją miR-204-3p a cechami kliniczno-patologicznymi, porównano obfitość miR-204-3p u pacjentów z BC z przerzutami do węzłów chłonnych lub bez nich. Dane ujawniły, że niższa ekspresja miR-204-3p była skorelowana z dodatnim przerzutem do węzłów chłonnych ( ryc. 1D ). Konsekwentnie, zmniejszoną ekspresję miR-204-3p zaobserwowano również u pacjentów z BC z większym rozmiarem guza ( ryc. 1E ). Wyniki te wykazały, że miR-204-3p był obniżony w BC i związany ze złym rokowaniem pacjentów z rakiem.
RYSUNEK 1
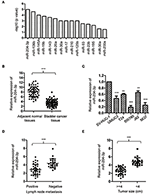
Rycina 1 . MiR-204-3p był obniżony w raku pęcherza moczowego. (A) Metaanaliza nieprawidłowo wyrażonych miRNA u pacjentów z rakiem pęcherza moczowego. (B) Ekspresję miR-204-3p w 60 sparowanych tkankach raka pęcherza moczowego i odpowiadających im sąsiednich normalnych tkankach określono za pomocą RT-qPCR. (C) Ekspresję miR-204-3p w komórkach raka pęcherza moczowego i prawidłowej komórce nabłonkowej pęcherza SV-HUC-1 określono na podstawie analizy RT-qPCR. (D) Ekspresję miR-204-3p u pacjentów z rakiem pęcherza z przerzutami do węzłów chłonnych lub bez nich określono za pomocą RT-qPCR. (E) Ekspresję miR-204-3p w tkankach raka pęcherza stratyfikowanych według wielkości guza określono za pomocą RT-qPCR. ** P <0,01 i ***P <0,001. RT-qPCR, ilościowa PCR z odwrotną transkryptazą.
Nadekspresja MiR-204-3p hamowała proliferację i indukowaną apoptozę komórek raka pęcherza moczowego
Ponieważ miR-204-3p był obniżony w BC, w celu zbadania wpływu nieprawidłowej ekspresji miR-204-3p na wzrost komórek BC, SW780 i 5637, które zawierały najniższą ekspresję miR-204-3p wśród wszystkich komórek testowane linie ( ryc. 1C ) transfekowano mimikami miR-204-3p w celu regulacji ekspresji miR-204-3p. Nadekspresję miR-204-3p zarówno w komórkach SW780, jak i 5637 wykryto za pomocą RT-qPCR ( ryc. 2A ). Wpływ miR-204-3p na proliferację komórek BC określono w teście CCK-8. Jak pokazano na rycinach 2B, C, wzrost zarówno komórek SW780, jak i 5637 został znacząco zahamowany przez nadekspresję miR-204-3p. Konsekwentnie, test tworzenia kolonii wskazał, że nadekspresja miR-204-3p drastycznie zmniejszyła liczbę kolonii w porównaniu z komórkami kontrolnymi ( ryc. 2D ). Ponadto, w celu dalszego potwierdzenia negatywnej regulacji nadekspresji miR-204-3p na wzrost komórek BC, zbadano wskaźnik apoptozy zarówno komórek SW780, jak i 5637 za pomocą analizy sortowania komórek aktywowanego fluorescencją (FACS). Wynik sugeruje, że ektopowa ekspresja miR-204-3p znacząco poprawiła apoptozę komórek BC ( ryc. 2E). Dane te wykazały, że nadekspresja miR-204-3p hamuje wzrost komórek BC, co sugeruje potencjalną funkcję supresji guza miR-204-3p w BC.
RYSUNEK 2
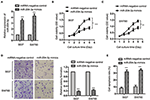
Rycina 2 . Nadekspresja miR-204-3p hamowała proliferację komórek raka pęcherza moczowego. (A) Ekspresję miR-204-3p zarówno w komórkach SW780, jak i 5637 z transfekcją miRNA naśladującą miR-204-3p lub kontrolnym miRNA potwierdzono za pomocą RT-qPCR. (B, C) Proliferację komórek za pomocą miR-204-3p naśladuje lub kontrolną transfekcję miRNA określono w teście CCK-8. (D) Test tworzenia kolonii przeprowadzono zarówno w komórkach SW780, jak i 5637 z transfekcją miR-204-3p naśladującą lub kontrolną miRNA. (E) Cytometrię przepływową przeprowadzono zarówno w komórkach SW780, jak i 5637 z transfekcją miR-204-3p lub kontrolnym miRNA. N = 3; ** P <0,01 i *** P<0,001. RT-qPCR, ilościowa PCR z odwrotną transkryptazą; CCK-8, Zestaw do liczenia komórek-8.
Dehydrogenaza mleczanowa była celem MiR-204-3p w komórkach raka pęcherza moczowego
Aby dalej badać leżący u podstaw mechanizm molekularny, za pomocą którego miR-204-3p moduluje wzrost komórek BC, cele miR-204-3p przewidywano przy użyciu bazy danych miRDB ( http://mirdb.org ). Wśród kandydatów stwierdzono, że LDHA jest możliwym celem miR-204-3p ( ryc. 3A). Aby potwierdzić potencjalne wiązanie między miR-204-3p z LDHA 3′-UTR (pozycja 515-521), WT lub MUT 3′-UTR LDHA zawierające przypuszczalne miejsca wiązania miR-204-3p wstawiono do wektor pmiR-GLO. Test reportera lucyferazy przeprowadzono przez kotransfekcję miRNA kontroli ujemnej lub miRNA 204-3p naśladuje WT lub MUT 3'-UTR LDHA. Wyniki pokazały, że nadekspresja miR-204-3p znacznie zmniejszyła aktywność lucyferazy WT3'-UTR LDHA; jednakże nie zaobserwowano znaczącego spadku, gdy komórki transfekowano MUT 3′-UTR LDHA ( Figury 3B, C ). Wynik ten wskazuje, że miR-204-3p wiąże 3'-UTR LDHA.
RYSUNEK 3
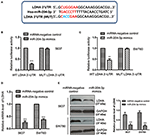
Rycina 3 . MiR-204-3p celował w LDHA w komórkach raka pęcherza moczowego. (A) Sekwencje komplementarne w 3'-UTR LDHA i miR-204-3p. (B, C) Wpływ miR-204-3p na aktywność lucyferazy dzikiego lub zmutowanego LDHA 3'-UTR określono w teście reporterowym lucyferazy. (D, E) Wpływ nadekspresji miR-204-3p na poziomy mRNA i białka LDHA zarówno w komórkach SW780, jak i 5637 potwierdzono odpowiednio w teście RT-qPCR i teście Western blot. N = 3; ** P <0,01 i *** P <0,001. LDHA, dehydrogenaza mleczanowa; UTR, region nieprzetłumaczony; RT-qPCR, ilościowa PCR z odwrotną transkryptazą.
Aby wykryć, czy wiązanie miR-204-3p w 3'-UTR wpłynęło na stabilność mRNA LDHA, zarówno komórki SW780, jak i 5637 transfekowano kontrolnymi naśladującymi miRNA lub miR-204-3p i zbadano poziom mRNA w LDHA za pomocą testu RT-qPCR. Jak pokazano na rycinie 3D , nadekspresja miR-204-3p znacznie obniżyła poziom mRNA LDHA w komórkach BC. Dodatkowo poziom białka LDHA w komórkach SW780 i 5637 wyrażających miR-204-3p badano również metodą Western blot przy użyciu przeciwciała anty-LDHA. Dane wykazały, że poziom LDHA był obniżony w wyniku transfekcji miR-204-3p w komórkach SW780 i 5637 ( ryc. 3E ). Wyniki te wykazały, że LDHA był celem miR-204-3p i był negatywnie regulowany przez miR-204-3p w komórkach BC.
MiR-204-3p tłumił glikolizę komórek raka pęcherza moczowego przez modulowanie dehydrogenazy mleczanowej
LDHA miała decydujące znaczenie dla metabolizmu glukozy w komórkach rakowych. Biorąc pod uwagę ujemną regulację miR-204-3p na ekspresję LDHA, wpływ miR-204-3p na glikolizę komórek BC określono przez pomiar zużycia glukozy i produkcji mleczanu. Wyniki wykazały, że nadekspresja miR-204-3p znacznie zmniejszyła wychwyt glukozy przez komórki SW780 i 5637 ( ryc. 4A ). Konsekwentnie, wytwarzanie mleczanu komórek BC zostało również dramatycznie zmniejszone w obecności wysokiego poziomu miR-204-3p ( Figura 4B ). Aby dodatkowo potwierdzić te wyniki, miR-204-3p został powalony w komórkach SW780 i 5637 przez transfekcję antagomiru miR-204-3p. Redukcja miR-204-3p została zweryfikowana za pomocą testu RT-qPCR ( ryc. 4C). Zbadano glikolizę komórek BC niosących zubożony miR-204-3p. Jak pokazano na rycinie 4D , regulacja w dół miR-204-3p znacznie zwiększyła zużycie glukozy zarówno w komórkach SW780, jak i 5637. Zwiększoną produkcję mleczanu uzyskano również przy zmniejszonej ekspresji miR-204-3p ( ryc. 4E ). Wyniki te wskazują, że miR-204-3p był ujemnym regulatorem glikolizy komórek BC.
RYSUNEK 4
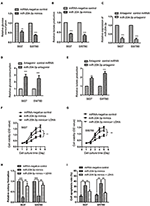
Rycina 4 . MiR-204-3p modulował glikolizę komórek raka pęcherza moczowego. (A, B) Komórki SW780 i 5637 transfekowano kontrolnymi naśladującymi miRNA lub miR-204-3p, i mierzono zużycie glukozy i produkcję mleczanu. (C) Ekspresję miR-204-3p w komórkach SW780 i 5637 z transfekcją antagomiru kontrolnego antagomiru lub miR-204-3p określono za pomocą RT-qPCR. (D, E) Wpływ powalenia miR-204-3p na pobieranie glukozy i wytwarzanie mleczanu przez komórki SW780 i 5637 określono odpowiednio za pomocą zestawu do oznaczania glukozy i zestawu do oznaczania mleczanu. (F, G) Żywotność komórek SW780 i 5637 z kotransfekcją miRNA i wektorami plazmidowymi określono za pomocą testu CCK-8. (H)Wzrost komórek SW780 i 5637 z kotransfekcją miRNA i wektorami plazmidowymi określono w teście tworzenia kolonii. (I) Apoptozę komórek SW780 i 5637 z kotransfekcją miRNA i wektorami plazmidowymi oceniano za pomocą cytometrii przepływowej. N = 3; ** P <0,01 i *** P <0,001. RT-qPCR, ilościowa PCR z odwrotną transkryptazą; CCK-8, Zestaw do liczenia komórek-8.
Aby dalej zbadać, czy za pomocą LDHA uzyskano hamujący wpływ miR-204-3p na proliferację komórek BC, przeprowadzono test CCK-8 przez transfekcję LDHA w komórkach z nadekspresją miR-204-3p. Wyniki wykazały, że wysoce wyrażona miR-204-3p hamuje proliferację i wzrost oraz indukuje apoptozę komórek zarówno komórek SW780, jak i 5637, a jednocześnie ratuje ekspresję LDHA osłabia hamujący wpływ miR-204-3p na wzrost proliferacji komórek BC i wzmocniony wpływ miR-204-3p na apoptozę komórek komórek BC ( ryc. 4F – I ). Dane te wykazały, że miR-204-3p zmniejszał ekspresję LDHA, hamował glikolizę i hamował wzrost komórek BC.
Dyskusja
Mimo znacznego postępu w leczeniu BC za pomocą chirurgii i chemioterapii, rokowanie w BC jest nadal złe. Ponadto większość pacjentów jest diagnozowana na zaawansowanym etapie i wykazuje niezadowalającą odpowiedź na leczenie. Warto zauważyć, że coraz więcej dowodów sugeruje, krytyczne miRNA rolę w inicjacji i progresji raka ( 9 - 11 ). Tutaj pokazaliśmy, że miR-204-3p był zmniejszony zarówno w tkankach BC, jak i liniach komórkowych, co było związane ze złym rokowaniem pacjentów z BC. Dalsza analiza wzmocnienia funkcji wykazała, że nadekspresja miR-204-3p hamuje wzrost komórek BC, co sugeruje potencjalną funkcję tłumiącą miR-204-3p w modulowaniu postępu BC.
Udział miR-204-3p w raku został podkreślony w badaniach, w których nieprawidłową ekspresję miR-204-3p można wykorzystać do rozróżnienia złośliwego postępu w raku żołądka ( 16 ) i raku piersi ( 26 ). Znaczący spadek miR-204-3p zaobserwowano w HCC, co tłumiło wzrost HCC poprzez celowanie w fibronektynę 1 ( 15 ). Ostatnie badania Chen i in. wykazał, że ksantohumol, prenylowany potencjał chalkonu w terapii przeciwnowotworowej, reguluje w górę ekspresję miR-204-3p w komórkach glejaka i indukuje apoptozę komórek poprzez modulowanie białka wiążącego insulinopodobny czynnik wzrostu (IGF) ( 27).). W jasnokomórkowym raku komórek nerkowych (ccRCC) stwierdzono, że miR-204-3p jest regulowany w dół przez tłumiony ERβ okrągły RNA ATP2B1, który zwiększał ekspresję fibronektyny 1 i promował inwazję komórek ccRCC ( 28).). Odkrycia te sugerują potencjalną funkcję supresji guza miR-204-3p w nowotworach. W niniejszym badaniu nasze dane ujawniły, że miR-204-3p był zmniejszony w tkankach BC w porównaniu z normalną tkanką. Regulacja w dół miR-204-3p była skorelowana z przerzutami do węzłów chłonnych i większym rozmiarem guza. Dalsze badania mogą być interesujące w celu zbadania związku między ekspresją miR-204-3p z 5-letnim całkowitym przeżyciem pacjentów z BC. Zgodnie ze zmniejszonym poziomem miR-204-3p w BC, nadekspresja miR-204-3p znacząco hamowała proliferację i indukowała apoptozę komórek BC. Test nowotworowy in vivo może być konieczny do dalszego potwierdzenia modulowania miR-204-3p na wzrost komórek BC w przyszłym badaniu.
Funkcję miRNA osiągnięto poprzez regulację ekspresji celów docelowych. W tym badaniu możliwe cele miR-204-3p zostały przewidziane przy pomocy bioinformatyki, a LDHA zidentyfikowano jako jednego z wiążących partnerów miR-204-3p. Nadekspresja miR-204-3p znacząco obniżyła zarówno poziom mRNA, jak i białka LDHA w komórkach BC. Konsekwentnie, nadekspresja miR-204-3p zmniejszała zużycie glukozy i produkcję mleczanu w komórkach BC. Niedobór LDHA powoduje zmniejszenie produkcji mleczanu, któremu towarzyszy hamowanie migracji komórek i inwazji. Dlatego LDHA była celem różnych miRNA w komórkach rakowych w celu regulacji nowotworu. Wśród nich stwierdzono, że miR-142-3p celuje w LDHA i hamuje tlenową glikolizę HCC ( 25). W raku piersi miR-30-5p hamował wzrost komórek i przerzuty poprzez hamowanie metabolizmu glukozy za pośrednictwem LDHA ( 29 ). Wyniki te łącznie wykazały, że przeprogramowanie glikolizy poprzez ukierunkowanie na LDHA było obiecującym sposobem modulowania postępu nowotworów.
Nasze badanie wciąż zawierało kilka ograniczeń. Po pierwsze, związek między miR-204-3p a całkowitym przeżyciem pacjentów z BC nie został określony w badaniu, które wymaga dalszych badań. Po drugie, w niniejszym badaniu brakuje badań na zwierzętach in vivo , a wpływ miR-203-3p na wzrost BC in vivo należy wziąć pod uwagę w przyszłych badaniach. Po trzecie, cele miR-204-3p nie były ograniczone do LDHA, a inne potencjalne cele mogą zostać zbadane w przyszłych badaniach.
Podsumowując, nasze wyniki wykazały, że miR-204-3p był obniżony w BC i korelował z postępem pacjentów z BC. Nadekspresja miR-204-3p zmniejszała wzrost komórek BC poprzez regulację w dół LDHA, co w konsekwencji tłumiło metabolizm glukozy w komórkach BC. Dane te wskazywały, że celowanie w szlak miR-204-3p-LDHA może zakłócać nowotworzenie komórek rakowych.
Oświadczenie o dostępności danych
Wszystkie zestawy danych dla tego badania są zawarte w artykule / materiale uzupełniającym.
Oświadczenie o etyce
Badania z udziałem ludzi zostały przejrzane i zatwierdzone przez Institutional Review Board of Shenzhen people's Hospital. Pacjenci / uczestnicy wyrazili pisemną świadomą zgodę na udział w tym badaniu.
Autorskie Wkłady
JG i KX zaprojektowali całe badanie. JG, PZ, ZLiu i ZLi przeprowadzili eksperymenty. YY, XZ i ZY przeprowadzili analizę statystyczną. JF i KX opracowali manuskrypt.
Finansowanie
Badanie to zostało wsparte przez granty z Sanming Project of Medicine w Shenzhen (SZSM201412014), Science and Technology Foundation of Shenzhen (JCYJ20170307095620828 i JCYJ20160422145718224) oraz Shenzhen Urology Minimal Invasive Engineering Center (GCZX2015043016165448). Wszystkie źródła finansowania otrzymane na przedłożone badania.
Konflikt interesów
Autorzy deklarują, że badanie zostało przeprowadzone przy braku jakichkolwiek powiązań handlowych lub finansowych, które można by interpretować jako potencjalny konflikt interesów.



Komentarze
Prześlij komentarz